1. Introduzione
2. EFFICACIA, SICUREZZA E TOSSICITÀ DEL BIOSSIDO DI CLORO


La pandemia di Covid-19 ha sconvolto il mondo e ha provocato migliaia di vittime e, tra le conseguenze altrettanto complicate, ha compromesso l’economia globale. Indubbiamente, si tratta di un problema che richiede una soluzione urgente e l’impegno di tutti, soprattutto del personale sanitario, per trovare una soluzione tempestiva.
Al fine di individuare una soluzione a questo problema e anche sulla base delle evidenze scientifiche già pubblicate e dell’esperienza clinica dell’utilizzo del diossido di cloro (ClO2) da parte di medici e ricercatori, abbiamo valutato le principali informazioni a sostegno della nostra proposta di utilizzare la soluzione di diossido di cloro (CDS), seguendo il protocollo standardizzato dal Dr. h.c. Andreas Ludwig Kalcker, come alternativa sicura ed efficace per combattere l’infezione da SARS-COV2.
Un’indagine di revisione sull’uso del diossido di cloro nella letteratura internazionale indicizzata è stata condotta da gennaio a luglio 2020 e, a titolo di esempio, se analizziamo solo il sito PubMed (National Library of Medicine 2020), osserviamo che solo utilizzando il descrittore “biossido di cloro”, abbiamo a disposizione un totale di 1.372 documenti datati dal 1933 alla data della ricerca, 2020 (Figura 1).
Un’altra fonte importante è stata la banca dati PubChem (Figura 2), nella quale è possibile individuare anche informazioni biochimiche e tossicologiche, tra le altre, e brevetti registrati (che possono essere trovati anche in Google Patents), tra cui i seguenti:
1) Il brevetto sulla disinfezione delle sacche di sangue (Kross & Scheer, 1991);
2) Il brevetto HIV (Kuhne 1993);
3) Il brevetto per il trattamento di malattie neurodegenerative come la sclerosi laterale amiotrofica (SLA), il morbo di Alzheimer e la sclerosi multipla (McGrath MS 2011);
4) Brevetto della Taiko Pharmaceutical (2008) per il coronavirus umano;
5) il brevetto su un metodo e una composizione “per il trattamento di tumori cancerosi” per il trattamento di tumori cancerosi (Alliger 2018);
6. brevetto per una composizione farmaceutica per il trattamento delle infiammazioni interne. (Kalcker LA, 2017);
7) il brevetto sulla composizione farmaceutica per il trattamento dell’avvelenamento acuto (Kalcker LA, 2017) e;
8) brevettare un composto farmaceutico per il trattamento di malattie infettive (Kalcker LA, 2017);
9) il brevetto sull’uso del CDS per il coronavirus di tipo 2 (Kalcker LA, 2020 – ancora in attesa di pubblicazione: /11136-CH_Antrag_auf_Patenterteilung.pdf).
Sulla base di questi soli dati iniziali, quindi, notiamo che la ricerca sulla ClO 2 Non si tratta di una novità, ma di una molecola chimica conosciuta da oltre 200 anni e commercializzata da 70 anni con una varietà di usi: trattamento dell’acqua per il consumo umano, trattamento delle acque contaminate, controllo del biofilm nelle torri di raffreddamento e nei processi di disinfezione di alimenti e vegetali.
Inoltre, esistono studi preclinici e clinici, nonché studi che ci permettono di capire le loro caratteristiche tossicologiche e di sicurezza soprattutto per l’uso umano (Lubbers et al 1984, Ma et al 2017).
La formula chimica del diossido di cloro è ClO2 e come registrato presso il Chemical Abstracts Services (CAS) della Chemical American Society il suo numero CAS è 10049-04-4. In questa formula, è evidente la presenza di un atomo di cloro (Cl) e di due atomi di ossigeno (O2) in una molecola di diossido di cloro. Questi 3 atomi sono tenuti insieme dagli elettroni per formare la molecola di ClO2. Può essere utilizzato come gas saturo di acqua distillata e può quindi essere bevuto o applicato direttamente sulla pelle e sulle mucose, con opportune diluizioni. Il Dr. h.c. Andreas Ludwig Kalcker, biofisico e ricercatore, ha standardizzato una saturazione di gas in acqua distillata chiamata soluzione di diossido di cloro o CDS (Chlorine Dioxide Solution): chlorine dioxide solution) (National Library of Medicine 2020).
La scoperta della molecola ClO2 nel 1814, è attribuita allo scienziato Sir Humphrey Davy. Il ClO2 è diverso dall’elemento cloro (Cl), sia nella sua struttura chimica e molecolare che nel suo comportamento. Il ClO2, come è stato ampiamente riportato, può avere effetti tossici se non si osservano le dovute precauzioni per i suoi vari usi e non si rispettano le raccomandazioni appropriate per il consumo umano. È noto che il ClO2 è tossico per l’uomo se inalato in forma pura e/o ingerito in quantità superiori a quelle raccomandate (Lenntech 2020, IFA 2020).
Il ClO2 è uno dei biocidi più efficaci contro agenti patogeni come batteri, funghi, virus, biofilm e altre specie di microrganismi che possono causare malattie. Agisce interrompendo la sintesi delle proteine della parete cellulare del patogeno. In quanto ossidante selettivo, la sua modalità d’azione è molto simile a quella della fagocitosi, dove un blando processo di ossidazione viene utilizzato per eliminare tutti i tipi di patogeni (Noszticzius et al 2013, Lenntech 2020). Vale la pena notare che il ClO2generato dal clorito di sodio (NaClO2), è approvato dalla Environmental Protection Agency negli Stati Uniti (EPA 2002) e dall’Organizzazione Mondiale della Sanità per l’uso nell’acqua potabile, in quanto non lascia residui tossici (EPA 2000, OMS 2002).
Se applicato alle concentrazioni appropriate, il ClO2 non forma prodotti alogenati e i loro sottoprodotti ClO2 sono normalmente entro i limiti raccomandati dall’EPA (2000, 2004) e dall’OMS (2000, 2002). A differenza del cloro gassoso, non si idrolizza facilmente e rimane nell’acqua come gas disciolto. Inoltre, a differenza del cloro, il ClO2 rimane in forma molecolare negli intervalli di pH comunemente presenti nelle acque naturali (EPA 2000, OMS 2002). L’OMS e l’EPA includono il ClO2 nel gruppo D (sostanze non classificabili come cancerogene per l’uomo) (IARC 2001, EPA 2009). Decondo il Dipartimento della Salute e dei Servizi Umani degli Stati Uniti 2004, la FDA raccomanda l’uso di ClO2 è consentito come additivo consentito negli alimenti e come agente antimicrobico (disinfettante).
Alcuni irresponsabili continuano a confondere il ClO2 con ipoclorito di sodio (NaClO – Candeggina) e il secondo con clorito di sodio (NaClO2), così come altri composti chimici, portando a frequenti commenti inappropriati sia nei media che tra i professionisti a causa della mancanza di conoscenze di chimica elementare. NaClO (candeggina), ad esempio, è un potente agente corrosivo e il pericolo dovuto all’esposizione cronica e massiccia a NaClO è ben noto. Si ritiene che i sintomi dell’asma sviluppati dai professionisti che lavorano a contatto con la sostanza possano essere dovuti all’esposizione continua alla candeggina, che è 300 volte più tossica della candeggina stessa. ClO2.
Sulla base di questa breve panoramica su cos’è il diossido di cloro e sulla sua capacità biocida, i risultati ottenuti dai medici dell’Associazione ecuadoriana di specialisti in medicina integrativa (AEMI) non sorprendono: che affermano che la somministrazione di CDS in diluizioni appropriate e sicure è un’alternativa efficace e a basso costo che può contribuire rapidamente al ripristino della salute dell’individuo infettato dal coronavirus umano di tipo 2, e si presume che possa favorire la riduzione della morbilità e della mortalità, ricoveri ospedalieri da COVID-19 per lo più fino a 4 giorni (AEMEMI 2020).
Attraverso le prove della letteratura scientifica disponibile che dimostrano l’efficacia del ClO2 per eliminare diversi patogeni (Kullai-Kály et al 2020), tra cui la SARS-CoV (Tabelle 1, 2, 3 e 4; Taiko Pharmaceutical Patent 2008), nonché i lavori che confermano la sicurezza dell’uso del biossido di cloro per la purificazione dell’acqua e, più recentemente, il già citato lavoro di AEMEMI, abbiamo valutato positivamente e con un grande potenziale biocida l’uso di ClO acquoso2 (CDS) per combattere i coronavirus (AEMEMI 2020, EPA 2000, OMS 2005, OMS 2002).
In questo contesto, ci sorprende che si menzioni che organismi ufficiali come Ministeri della Salute, PAHO/OMS e agenzie regolatorie e/o enti sanitari non raccomandino l’uso di ClO2 e tutti, invece di raccomandare, richiamano l’attenzione sulla sua tossicità e pericolosità, ma, nei loro interventi, non indicano chiaramente in quale forma, dosaggio e per quale via di somministrazione il ClO2 è davvero tossico. Tuttavia, tutto ci porta a capire che si riferiscono alla forma pura e concentrata di questo gas nell’aria e non alla formula standardizzata dal Dr. Kalcker: la soluzione acquosa di diossido di cloro (CDS), a 3.000 ppm.
Alla luce del grave scenario a cui il mondo intero è stato esposto con la pandemia da coronavirus, rivolgiamo le seguenti domande alle autorità e alle istituzioni responsabili della salute umana a capo delle principali istituzioni:
Per lo scopo legalmente stabilito di salvare vite umane, non è logicoNon è salutare, né tanto meno un’azione umanitaria e compassionevole, di fronte a un’emergenza pubblica globale, che si producano equivoci nella traduzione delle conoscenze scientifiche per qualsiasi scopo che non sia la salvaguardia della vita. Riteniamo che questi fraintendimenti possano essere causati da una scarsa conoscenza della letteratura esistente (nonostante sia aperta alla consultazione pubblica). Ricordiamo che solo nel database PubMed ci sono più di 1.300 articoli pubblicati utilizzando il solo descrittore “biossido di cloro”.
Supponendo che i team incaricati di redigere i documenti ufficiali, gli articoli, i rapporti pubblicati sui siti web di organismi ufficiali come PAHO/OMS dei Paesi membri, Ministeri della Salute e organismi di regolamentazione sanitaria, non fossero a conoscenza degli articoli e dei brevetti (il che non li esime dalla responsabilità legale) che dimostrano la non tossicità a queste dosi e i possibili benefici del biossido di cloro per la salute umana e che, quindi, questi team incaricati non abbiano ancora considerato il potenziale del biossido di cloro per la salute umana.2 Nella lotta contro il coronavirus di tipo 2, come hanno fatto AEMEMI e il team di Medici e Ricercatori che hanno firmato questo dossier, vi invitiamo a riflettere su quanto segue:
Sulla base delle informazioni dissonanti e incoerenti rispetto alle reali conoscenze sui CDS e sulle loro potenzialità, noi professionisti della salute intendiamo dare rispettosamente il nostro contributo affinché le istituzioni sanitarie rivedano la loro documentazione e le linee guida ufficialmente pubblicate per promuovere informazioni più chiare e veritiere sull’uso, l’efficacia e la sicurezza del ClO2 per il consumo umano orale (CDS), come standardizzato da Kalcker (2020 – Informazioni sulla valutazione: /11136-CH_Antrag_auf_Patenterteilung.pdf), Di seguito riportiamo una sintesi dei fatti e delle prove scientifiche principali che dimostrano l’efficacia dei CDS contro diversi agenti patogeni, tra cui il coronavirus umano di tipo 2, l’agente causale della SARS-CoV2.
Purtroppo, il modo in cui le informazioni sul ClO2genera falsi dubbi e soprattutto rivela a chi comprende l’argomento da un punto di vista scientifico che la disinformazione generata sembra essere deliberatamente pianificata.
Più di 17 anni fa, Andreas Ludwig Kalcker ha avviato una ricerca scientifica per studiare l’applicabilità del ClO2 e le sue diluizioni, in modo che possa essere utilizzato in modo sicuro per il consumo umano. Sulla base di questi studi, ha sviluppato 4 brevetti, di cui 3 pubblicati e uno in attesa di approvazione. Questi studi si basano sui livelli di tossicità sicuri stabiliti dalla banca dati tedesca di tossicologia Gestis (IFA 2020) e tengono conto di altri studi di riferimento già sviluppati, ad esempio dall’OMS (2000, 2005) e dall’EPA (2000).
Questi studi confermano la non tossicità di questo gas in soluzione acquosa per il consumo umano e stabiliscono, ad esempio, che la dose sicura è di 0,3 mg/L da utilizzare per l’acqua potabile. Gli studi di Kalcker e le esperienze cliniche dei medici raccomandano l’utilizzo di 10 mL di questa soluzione concentrata, diluita in 1000 mL di acqua, come uno dei protocolli per combattere la SARS-COV 2. In questa specifica raccomandazione, alla fine è consentito il consumo di 30 mg/die, suddivisi in 10 dosi da 100mL, che risulta sicuro e non tossico sulla base di riferimenti scientifici riconosciuti (Lubbers & Bianchine 1984; Ma et al 2017)..
Polemiche inutili e loro conseguenze
Storicamente, un prodotto chiamato “soluzione minerale miracolosa” (MMS) è stato oggetto di molte controversie nei media di tutto il mondo perché venduto come “medicina”.
Su Internet si trovano spesso notizie che confondono la “soluzione minerale miracolosa” (MMS = acido citrico + clorito di sodio + acqua) con la “soluzione di biossido di cloro” (CDS = acido cloridrico + clorito di sodio + acqua) e quest’ultima con l’ipoclorito di sodio (candeggina). Le principali differenze tra MMS e CDS sono riportate nella tabella 1:
Caratteristiche generali | MMS | CDS |
Concentrazione di ClO2 (parte per milione – ppm) | Non conosciuto | 3.000 ppm |
Ph | Ácido | Neutro (7) |
Residuo | Clorati, cloruro | Senza rifiuti |
Le conseguenze e l’impatto di questi fallimenti nella traduzione delle conoscenze scientifiche in un momento di emergenza sanitaria globale, quando la vita di molte persone è a rischio, sono preoccupanti.
Pertanto, è urgente che tutte le istituzioni siano attente attraverso la qualificazione preventiva delle informazioni che vengono pubblicate, in modo che non ci siano difetti nella traduzione delle conoscenze scientifiche, generando così spazio per dubbi e interpretazioni errate attraverso i media, con gravi conseguenze e influenzando negativamente il processo decisionale dei manager.
Se utilizzassimo ipoclorito di sodio (NaClO) con acido cloridrico nell’acqua, la soluzione conterrebbe Cl2 + NaCl + H2O. El Cl2 eè un gas tossico che reagisce con le sostanze organiche, soprattutto in ambiente acquoso, dove può formare acidi tossici.
Sebbene siano chiare le differenze biochimiche consolidate, molti continuano a confondere alcune sostanze chimiche con il ClO2 (Tabella 2):
COMPOSTI CHIMICI | |||||||
| CARATTERISTICHE BIOCHIMICHE | Perclorato di sodio | Clorato di sodio | Clorito di sodio | Ipoclorito di sodio | Cloruro di sodio | Cloro | Dióssido de cloro |
| Struttura | 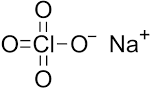 | 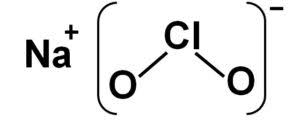 | 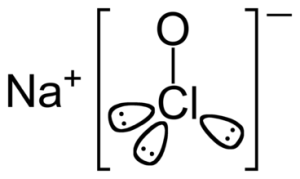 | 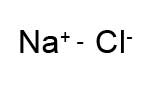 |  | 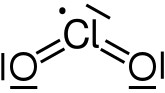 | |
| Formula chimica | NaClO4 | NaClO3 | NaClO2 | NaClO | NaCl | Cl2 | ClO2 |
| Peso molecolare | 122.44 g/mol | 106.44 g/mol | 90.44 g/mol | 74.44 g/mol | 58.44 g/mol | 70.9 g/mol | 67.45 g/mol |
La maggior parte dei virus si comporta in modo simile perché, una volta infettata la cellula, l’acido nucleico del virus assume la sintesi delle proteine della cellula.
Alcuni segmenti dell’acido nucleico del virus sono responsabili della replicazione del materiale genetico del capside (spiga), una struttura che ha la funzione di proteggere il genoma virale durante il suo trasferimento da una cellula all’altra e di assistere il trasferimento tra le cellule ospiti.
Quando il ClO2 incontra un virus o una cellula infetta, si verifica un processo di denaturazione molto simile alla fagocitosi, poiché si tratta di un ossidante selettivo (Noszticzius et al 2013).
Studi preclinici che esplorano la tossicità del ClO2 di solito non si riscontrano effetti negativi quando gli animali sono esposti a diverse concentrazioni di questo biocida. Alcuni dei più importanti sono elencati di seguito. Ogata (2007) ha esposto 15 ratti a 0,03 ppm di ClO2 gassoso per 21 giorni.
L’esame microscopico dei campioni istopatologici prelevati dai polmoni di questi ratti ha mostrato che i loro polmoni erano “completamente normali”. In un altro studio preclinico, Ogata et al. (2008) hanno esposto ratti a 1 ppm di ClO2 gas per 5 ore al giorno, 5 giorni alla settimana per un periodo di 10 settimane. Non sono stati osservati effetti avversi. Hanno concluso che il “livello di non effetto avverso osservato” (NOAEL) per il biossido di cloro gassoso è di 1 ppm, un livello ritenuto non tossico per gli esseri umani e superiore alla concentrazione di 0,03 ppm riportata per proteggere dall’infezione da virus influenzale.
In studi sui ratti, Haller e Northgraves (1955) hanno riscontrato che l’esposizione a lungo termine (2 anni) a 10 ppm di diossido di cloro non ha prodotto effetti negativi. Tuttavia, i ratti esposti a 100 ppm hanno mostrato un aumento del tasso di mortalità.
Musil et al (2004) hanno riportato che dosi elevate (200-300 mg/kg) di clorito di sodio causano l’ossidazione dell’emoglobina a metaemoglobina. Tuttavia, quando i ratti hanno bevuto per 40 giorni acqua con livelli variabili di diossido di cloro (da 0,175 a 5 ppm), non sono stati osservati cambiamenti nei parametri ematologici. In un altro studio, polli e ratti che hanno bevuto quotidianamente biossido di cloro nell’acqua potabile a concentrazioni fino a 1000 ppm per 2 mesi non hanno prodotto metaemoglobina. Richardson (2004) ha riportato che dosi elevate di clorato di sodio (NaClO₃) per via orale (che non è la stessa cosa del clorito di sodio – NaClO₃) (che non è la stessa cosa del clorito di sodio – NaClO₃) erano associate a livelli elevati di cloruro di sodio.2) ClO2 produce metaemoglobinemia e nefrite (US Department of health and human service, 2004).
Fridliand & Kagan (1971) hanno riportato che i ratti che consumavano per via orale 10 ppm di ClO2 per 6 mesi non ha avuto effetti negativi sulla salute. Quando l’esposizione è stata aumentata a 100 ppm, l’unica differenza tra il gruppo di trattamento e quello di controllo è stato un aumento di peso più lento nel gruppo di trattamento. Nel tentativo di simulare lo stile di vita umano convenzionale, Akamatsu et al. (2012) hanno esposto dei ratti al gas di biossido di cloro a una concentrazione di 0,05 – 0,1 ppm, 24 ore al giorno, 7 giorni alla settimana per un periodo di 6 mesi. Hanno concluso che per i ratti l’esposizione del corpo intero al biossido di cloro fino a 0,1 ppm per un periodo di 6 mesi non è tossica.
Dosi più elevate di ClO2 (ad es. 50-1000 ppm) può causare alterazioni ematologiche negli animali, tra cui diminuzione dei globuli rossi, metaemoglobinemia e anemia emolitica in caso di respirazione prolungata. Livelli ridotti di tiroxina nel siero sono stati osservati anche in scimmie esposte a 100 ppm nell’acqua potabile e in cuccioli di ratto esposti a concentrazioni fino a 100 ppm tramite gavage o indirettamente attraverso l’acqua potabile delle loro madri (US Department of health and human service, 2004). Tuttavia, dosi eccessive causano un cattivo sapore e le scimmie logicamente bevono meno acqua, cosa che non ha trovato riscontro negli studi.
Moore e Calabrese (1982) hanno studiato gli effetti tossicologici del ClO2 nei ratti e hanno osservato che quando i ratti sono stati esposti a un livello massimo di 100 ppm attraverso l’acqua potabile e né i ratti A/J né i C57L/J hanno mostrato nessuna alterazione ematologica. È stato inoltre riscontrato che i ratti esposti fino a 100 ppm di clorito di sodio (NaCIO2) nell’acqua potabile per un massimo di 120 giorni non hanno mostrato alcun cambiamento istopatologico nella struttura dei reni.
Shi e Xie (1999) hanno indicato che un valore di DL50 orale acuta (che dovrebbe portare alla morte del 50% degli animali dosati) per il biossido di cloro stabile era di >10.000 mg/kg nei topi. Nei ratti, i valori della DL50 orale acuta per il clorito di sodio (NaClO2) variava da 105 a 177 mg/kg (equivalente a 79-133 mg di clorito/kg) (Musil et al 1964, Seta et al 1991). Non sono stati osservati decessi dovuti all’esposizione in ratti che hanno ricevuto biossido di cloro nell’acqua potabile per 90 giorni a concentrazioni che hanno portato a dosi fino a circa 11,5 mg/kg/die nei maschi e 14,9 mg/kg/die nelle femmine (Daniel et al 1990).
Secondo l’Agenzia per la Protezione dell’Ambiente (EPA) degli Stati Uniti, la tossicità a breve termine della ClO2 è stato valutato in studi sull’uomo da Lubbers et al (1981, 1982, 1984a e Lubbers & Bianchine 1984c). Nel primo studio (Lubbers et al 1981, pubblicato anche come Lubbers et al 1982), un gruppo di 10 uomini adulti sani ha bevuto 1.000 mL (divisi in due porzioni da 500 mL, separate da 4 ore) di una soluzione di biossido di cloro a 0 o 24 mg/L (0,34 mg/kg, assumendo un peso corporeo di base di 70 kg). Nel secondo studio (Lubbers et al 1984a), gruppi di 10 uomini adulti hanno ricevuto 500 mL di acqua distillata contenente 0 o 5 mg/l di ClO2 (0,04 mg/kg al giorno, assumendo un peso corporeo di base di 70 kg) per 12 settimane.
Nessuno studio ha rilevato cambiamenti fisiologicamente rilevanti nella salute generale (osservazioni ed esame fisico), nei segni vitali (pressione sanguigna, frequenza del polso, frequenza respiratoria e temperatura corporea), nei parametri chimici clinici del siero (compresi i livelli di glucosio, azoto ureico e fosforo), nella fosfatasi alcalina e nell’aspartato e alanina aminotransferasi), nella triiodotironina (T3) e nella tiroxina (T4) del siero o nei parametri ematologici (EPA, 2004).
Michael et al (1981), Tuthill et al (1982), e Kanitz et al (1996) hanno esaminato gli effetti dell’acqua potabile disinfettata con ClO2. Michael et al. (1987) non hanno riscontrato anomalie significative nei parametri ematologici o nella chimica del siero. Tuthill e collaboratori (1982) hanno confrontato retrospettivamente i dati sulla morbilità e mortalità neonatale in due comunità: una che utilizzava il cloro e l’altra che lo utilizzava. ClO2 per purificare l’acqua. Esaminando questo studio, l’EPA non ha riscontrato differenze tra queste comunità (US Department of Health and Human Service, 2004).
Kanitz et al. (1996) hanno studiato le nascite in due ospedali italiani in cui l’acqua era purificata con cloro o ClO2. Sebbene gli autori abbiano concluso che i neonati nati da madri che hanno consumato acqua potabile trattata con ClO2 Tuttavia, l’EPA ha scritto che le variabili confondenti precludevano la possibilità di trarre conclusioni da questo studio (US Department of Health and Human Service, 2004).
La sopravvivenza non è risultata significativamente ridotta in gruppi di ratti esposti al clorito (come il clorito di sodio) nell’acqua potabile per due anni a concentrazioni che hanno portato a dosi stimate di clorito fino a 81 mg/kg/giorno.
In un altro studio, Kurokawa et al. (1986) hanno riscontrato che la sopravvivenza non era influenzata negativamente nei ratti che ricevevano clorito di sodio nell’acqua potabile a concentrazioni che risultavano in dosi stimate di clorito fino a 32,1 mg/kg/die nei maschi e 40,9 mg/kg/die nelle femmine”.
L’esposizione di ratti al clorito di sodio per un massimo di 85 settimane, a concentrazioni che hanno portato a dosi stimate di clorito fino a 90 mg/kg/giorno, non ha influito sulla sopravvivenza (Kurokawa et al. 1986).
Secondo Lubbers et al 1981, non ci sono stati segni di effetti epatici avversi (valutati attraverso test di chimica del siero) in maschi adulti che hanno consumato ClO2 in soluzione acquosa, con una dose di circa 0,34 mg/kg o in altri maschi adulti che consumano circa 0,04 mg/kg/die per 12 settimane. Gli stessi ricercatori hanno somministrato clorito a uomini adulti sani e non hanno riscontrato alcuna evidenza di effetti avversi sul fegato dopo che ciascun individuo ha consumato un totale di 1.000 mL di una soluzione contenente 2,4 mg/L di clorito (circa 0,068 mg/kg) in due dosi (separate da 4 ore), o in altri uomini normali o con deficit di G6PD che hanno consumato circa 0,04 mg/kg/die per 12 settimane (Lubbers et al 1984a, 1984b).
Non sono stati osservati segni di compromissione della funzionalità epatica. indotto dalla ClO2 o clorite tra gli abitanti dei villaggi rurali che sono stati esposti per 12 settimane attraverso il ClO2 nell’acqua potabile in concentrazioni settimanali da 0,25 a 1,11 mg/L (ClO2) o da 3,19 a 6,96 mg/L (clorite) (Michael et al 1981). In questo studio epidemiologico, i livelli di ClO2 nell’acqua potabile prima e dopo il periodo di trattamento. <0,05 mg/L. Il livello di clorito nell’acqua potabile era pari a 0,32 mg/L prima del trattamento con ClO2. Una settimana e due settimane dopo l’interruzione del trattamento, i livelli di clorito sono scesi rispettivamente a 1,4 e 0,5 mg/l.
Nel suo documento ufficiale intitolato “Laboratory Biosafety Manual” (pag. 93), l’OMS (2005) parla del ClO2:
“Diossido di cloro (ClO2) è un germicida, disinfettante e ossidante potente e ad azione rapida, solitamente attivo a concentrazioni inferiori a quelle richieste per la candeggina a base di cloro. La forma gassosa è instabile e si decompone in cloro gassoso. (Cl2) e ossigeno gassoso (O2), produrre calore. Tuttavia, il ClO2 è solubile in acqua e stabile in soluzione acquosa.
In genere si può ottenere in due modi:
(1) Per generazione in loco, mescolando due diversi componenti, acido cloridrico (HCl) e clorito di sodio. (NaClO2) come miscela.
2) Generato in forma stabilizzata, che viene attivato elettroliticamente in acqua in laboratorio.
Il ClO2 è il più selettivo tra i biocidi ossidanti. L’ozono e il cloro sono molto più reattivi del cloro.l ClO2 e reagiscono con la maggior parte dei composti organici.
Al contrario, il ClO2 solo reagisce con i composti dello zolfo ammine ridotte, secondarie e terziarie e altri composti organici altamente ridotti e reattivi.
Pertanto, con il ClO2 si possono ottenere meno residui ed è più stabile a dosi molto più basse rispetto all’uso del cloro o dell’ozono. Se generato correttamente, il file ClO2, Grazie alla sua selettività, può essere utilizzato più efficacemente dell’ozono o del cloro nei casi di maggiore carico di materia organica”.
Sulla base della Strategia dell’OMS sulla Medicina Tradizionale 2014-2023 (OMS 2013), che riconosce le pratiche legate alla medicina tradizionale, complementare e integrativa o “non convenzionale” come una parte importante dei servizi sanitari, al fine di integrarli costantemente con i vari Paesi membri firmatari di questa iniziativa, poniamo qui il potenziale della soluzione acquosa di ClO2 (Kalcker 2017) come potente biocida e quindi come alternativa complementare sicura per combattere la SARS-CoV2.
Il ClO2 è in grado di combattere i virus attraverso il processo di ossidazione selettiva mediante la denaturazione delle proteine del capside e la successiva ossidazione del materiale genetico del virus, rendendolo inattivo. Poiché non è possibile un adattamento del virus al processo di ossidazione, è impossibile che il virus sviluppi una resistenza al processo di ossidazione. ClO2, diventa un trattamento promettente per qualsiasi ceppo di virus.
Esistono prove scientifiche sufficienti che il ClO2 è efficace contro il coronavirus SARS-CoV-2 e altri:
Aparicio et. al. al. (trilogia) ha dimostrato in più di 3000 persone la sua efficacia nella prevenzione, nel trattamento e nelle sequele (Long covid) della Sars Cov-2, dove ha potuto dimostrare in 1136 pazienti infetti e con sintomi di Covid un’efficacia del 99,3% con un tempo medio di recupero di 4 giorni.
Wang e collaboratori (2005) studieranno le condizioni di persistenza del SARS-CoV-2 in diversi ambienti e la sua completa inattivazione per effetto di ossidanti quali ClO2Il Dipartimento di Microbiologia e Medicina dell’Università del New England ha studiato l’inattivazione di rotavirus umani e scimmieschi (SA-11) da parte della ClO2. Gli esperimenti sono stati condotti a 4°C in tampone fosfato-carbonato standard. Entrambi i virus sono stati rapidamente inattivati in soli 20 secondi in condizioni alcaline con concentrazioni di ClO2 da 0,05 a 0,2 mg/L (Chen & Vaughn 1990);
L’Università giapponese di Tottori ha valutato l’attività antivirale del ClO2 in soluzione acquosa e ipoclorito di sodio contro il virus dell’influenza umana, il morbillo, il virus della distemperosi canina, l’herpesvirus umano, l’adenovirus umano, l’adenovirus canino, il calicivirus felino e il parvovirus canino;
Il ClO2 a concentrazioni comprese tra 1 e 100 ppm ha prodotto una potente attività antivirale, inattivando > o = 99,9% dei virus in soli 15 secondi di trattamento. L’attività antivirale di ClO2 era circa 10 volte superiore a quello di NaClO (Sanekata et al 2010).
L’Università italiana di Parma ha condotto studi sull’inattivazione di virus resistenti agli agenti ossidanti, come il coxsackievirus, il virus dell’epatite A (HAV) e il calicivirus felino: i dati ottenuti dagli studi mostrano quanto segue: Per la completa inattivazione di HAV e calicivirus felino sono necessarie concentrazioni. > o = 0,6 mg/L. Test simili per il Coxsackie B5 hanno dato gli stessi risultati. Tuttavia, per il calicivirus felino e l’HAV, a basse concentrazioni di disinfettante, sono necessari circa 20 minuti per ottenere una riduzione del 99,99% della carica virale (Zoni et al 2007);
L’Istituto di Salute Pubblica e Medicina Ambientale di Tainjin, in Cina, ha condotto uno studio per chiarire i meccanismi di inattivazione del virus dell’epatite A (HAV) attraverso l’utilizzo di ClO2, osservando la completa distruzione dell’antigenicità dopo 10 minuti di esposizione con 7,5 mg di ClO2 per litro (Li et al 2004);
Il Dipartimento di Biologia dell’Università Statale del New Mexico (USA) ha condotto uno studio sull’inattivazione del poliovirus con ClO2 e iodio. Ha concluso che il ClO2 inattiva il poliovirus reagendo con l’RNA virale e influenzando la capacità del genoma virale di fungere da modello per la sintesi di RNA (Alvarez ME & O’Brien RT 1982). Taiko Pharmaceutical Co., Ltd., Seikacho, Kyoto, Giappone ha dimostrato in questo studio che il gas ClO2 in concentrazioni estremamente basse, senza alcun effetto nocivo sulla salute umana, produce un forte effetto disattivante su batteri e virus, riducendo significativamente la quantità di microbi vitali nell’aria di un centro chirurgico ospedaliero (Taiko Pharmaceutical 2016).ClO2
La tossicità DL50 (indice di tossicità acuta) stabilita dalla banca dati tedesca di tossicologia GESTIS per la ClO2 è di 292 mg per chilogrammo per 14 giorni, mentre l’equivalente per un adulto di 50 kg sarebbe di 15.000 mg per 14 giorni (IFA 2020). Secondo il Dipartimento della Salute e dei Servizi Umani degli Stati Uniti, il valore di ClO2 agisce rapidamente quando entra nel corpo umano. Il ClO2 si trasforma rapidamente in ioni clorite, che a loro volta si decompongono in ioni cloruro. L’organismo utilizza questi utili ioni per molti scopi elementari. Questi ioni cloruro (sale comune) lasciano l’organismo in poche ore o giorni, principalmente attraverso l’urina (EPA 1999).
La tossicità a breve termine del ClO2 è stato valutato in studi sull’uomo dai gruppi di ricerca di Lubbers et al:
Nel primo studio (Lubbers et al 1981; pubblicato anche come Lubbers et al 1982), un gruppo di 10 uomini adulti sani ha bevuto 1.000 mL (divisi in due porzioni da 500 mL, separate da 4 ore) di una soluzione di ClO2 24 mg/L (0,34 mg/kg, assumendo un peso corporeo di riferimento di 70 kg). Nel secondo studio (Lubbers et al 1984a), a gruppi di 10 uomini adulti sono stati somministrati 500 mL di acqua distillata contenente 0 o 5 mg/kg al giorno di ClO2 (0,04 mg/kg al giorno, assumendo un peso corporeo basale di 70 kg) per 12 settimane. Nessuno studio ha rilevato cambiamenti fisiologicamente rilevanti nella salute generale (osservazioni ed esame fisico), nei segni vitali (pressione sanguigna, frequenza del polso, frequenza respiratoria e temperatura corporea), nei parametri chimici clinici del siero (compresi i livelli di glucosio, azoto ureico e fosforo), nella fosfatasi alcalina e nell’aspartato e alanina aminotransferasi), nella triiodotironina (T3) e nella tiroxina (T4) del siero o nei parametri ematologici (EPA 2000).
Ma et al (2017) hanno valutato l’efficacia e la sicurezza di una soluzione acquosa di ClO2 contenente 2.000 ppm. L’attività antimicrobica è stata del 98,2% a concentrazioni comprese tra 5 e 20 ppm per batteri fungini e virus H1N1. In un test di tossicità per inalazione, 20 ppm di ClO2 per 24 ore non ha mostrato mortalità o anomalie nei sintomi clinici e/o nella funzionalità polmonare e di altri organi. Un raduno di CLO2 fino a 40 ppm nell’acqua potabile non ha mostrato alcuna tossicità orale subcronica.
Taylor e Pfohl, 1985; Toth et al., 1990), Orme et al., 1985; Taylor e Pfohl, 1985; Mobley et al., 1990) hanno studiato la tossicità del biossido di cloro su vari organi corporei in diversi stadi di sviluppo negli esemplari animali studiati e hanno riportato un Lowest Observed Adverse Effect Level (LOAEL) per questi effetti di 14 mg kg-1 giorno-1 di diossido di cloro.
Mentre Orme et al. (1985) hanno identificato un livello di effetti avversi non osservati (NOAEL) pari a 3 mg kg-1 giorno-1. L’esperienza clinica di oltre 5.000 medici COMUSAV in America Latina negli ultimi due anni suggerisce che l’ingestione di 30 mg al giorno di diossido di cloro disciolti in un litro d’acqua e bevuti per dieci volte nell’arco della giornata è un trattamento efficace per la COVID-19, che è 14 volte inferiore alla dose considerata come LOAEL.
Pertanto, l’ampia revisione della letteratura conferma che l’uso del diossido di cloro ingerito alla dose di 50 mg/die in un adulto non comporta sicuramente un rischio di tossicità per la salute umana per ingestione e rappresenta un trattamento molto efficace per la COVID-19.
Sulla base dell’esperienza medica, abbiamo fatto le seguenti osservazioni:
I progressi e le scoperte scientifiche sono costanti e, nel campo della salute, il loro rapido accesso da parte del personale sanitario e dei pazienti diventa essenziale e urgente, rendendo logico e obbligatorio, per puro senso umanitario e secondo il rigore scientifico, testare sostanze come il Diossido di Cloro (ClO2) per i quali è stata dimostrata l’efficacia e l’utilità. In tutta la storia della medicina, la supremazia del criterio del “Ricorso compassionevole”. rispetto al criterio della “risorsa consolidata”.
Gli articoli 32 e 37 della Dichiarazione di Helsinki del 1964 lo consentono nel caso di “Interventi non provati”.»(INC),“Quando nella cura di un paziente non esistono interventi comprovati o altri interventi conosciuti si sono dimostrati inefficaci, il medico, dopo aver chiesto il parere di esperti, con il consenso informato del paziente o di un rappresentante legalmente autorizzato, può essere autorizzato a utilizzare interventi non comprovati se, a giudizio del medico, questo dà qualche speranza di salvare la vita, ripristinare la salute o alleviare la sofferenza”.
I medici, in conformità con la Dichiarazione di Ginevra del 1948, quando si trovano di fronte a pazienti la cui salute e vita sono in pericolo, devono l’obbligo di utilizzare tutti i mezzi e i prodotti disponibili a loro disposizione, che mostrano segni di efficacia e in misura ancora maggiore in caso di emergenza medica, poiché l’uso del biossido di cloro (ClO2), la cui atossicità è stata documentata e la cui efficacia e sicurezza sono state dimostrate in studi e pratiche condotti in diversi Paesi.
Allo stesso modo, gli Stati, le Istituzioni e le Organizzazioni non possono limitarne o impedirne l’uso a fronte delle evidenze cliniche esistenti, altrimenti violerebbero gli obblighi assunti nei testi internazionali e nazionali, incorrendo nella violazione di diritti fondamentali come il diritto alla vita e salute, nonché la il diritto del paziente all’autodeterminazione e l’autonomia professionale e l’indipendenza clinica.
In conformità a quanto sopra, l’esercizio della professione medica implica una vocazione di servizio all’umanità, la cui massima preoccupazione è la salute e la vita del paziente, e deve garantire il beneficio degli interessi dei cittadini, mettendo a loro disposizione le conoscenze mediche nel quadro dell’autonomia professionale e dell’indipendenza clinica. Nell’ambito dell’attuale quadro normativo, pienamente applicabile ed esigibile, la professione medica deve avere a disposizione libertà professionale senza interferenze nell’assistenza e nel trattamento dei pazienti, avendo il privilegio di utilizzare il proprio giudizio professionale e la propria discrezione nel prendere decisioni cliniche e eticanecessaria.
I medici sono legalmente dotati di un elevato grado di autonomia professionale e di indipendenza clinica, per cui possono formulare raccomandazioni basate sulle loro conoscenze ed esperienze, sulle evidenze cliniche e sulla comprensione olistica dei pazienti, compreso ciò che è meglio per loro. senza influenze esterne indebite o inappropriatee adottare misure appropriate per garantire l’esistenza di sistemi efficaci.
Ogni paziente ha il diritto di essere assistito da un medico che sa essere libero di fornire un trattamento adeguato. giudizio clinico ed etico, senza alcuna interferenza esterna. Il paziente ha il diritto all’autodeterminazione e a prendere liberamente le decisioni che lo riguardano. I pazienti, nel libero esercizio del loro diritto all’autonomia, hanno il diritto di disporre del proprio corpo e le loro decisioni devono essere rispettate, essendo pienamente tutelati per evitare che terzi intervengano sul loro corpo senza il loro consenso, e devono essere adeguatamente informati sullo scopo dell’intervento, la sua natura, i rischi e le conseguenze.
Il diritto alla salute richiede che i governi adempiano agli obblighi previsti dai patti per rendere disponibili beni e servizi sanitari in quantità sufficiente, con accesso pubblico e di buona qualità, in conformità con il Commento generale 14 del Comitato sui diritti economici, sociali e culturali.
Tutto questo è coperto dalle disposizioni elencate di seguito, i cui contenuti essenziali sono riassunti di seguito;
Il Patto internazionale sui diritti economici, sociali e culturali del 16 dicembre 1966, firmato dall’Ecuador il 24 settembre 1968 e ratificato l’11 giugno 2010, riconosce il diritto di ogni individuo a godere del più alto livello raggiungibile di salute fisica e mentale; articolo 12 “…”.1. Gli Stati parti del presente Patto riconoscono il diritto di ogni individuo a godere del più alto livello raggiungibile di salute fisica e mentale”.1. Gli Stati parti del presente Patto riconoscono il diritto di ogni individuo a godere del più alto livello raggiungibile di salute fisica e mentale”.
1.“Ogni Stato parte del presente Patto si impegna a prendere misure, individualmente e attraverso l’assistenza e la cooperazione internazionale, specialmente economica e tecnica, al massimo delle sue risorse disponibili, al fine di raggiungere progressivamente la piena realizzazione dei diritti riconosciuti nel presente Patto con tutti i mezzi appropriati, compresa in particolare l’adozione di misure legislative.”
Il Codice Internazionale di Etica Medica dell’ottobre 1949, al fine di dare attuazione, tra l’altro, agli articoli 36 e 59 di tale testo;
Articolo 36 del Capitolo VII sulle cure di fine vita.
“1. Il medico ha il dovere di cercare di curare o migliorare il paziente, quando possibile. Quando non lo è più, resta l’obbligo di attuare misure adeguate per garantirne il benessere, anche se ciò può comportare una riduzione della vita.
2. Il medico non deve intraprendere o continuare azioni diagnostiche o terapeutiche che siano dannose per il paziente, senza speranza di beneficio, futili o ostinate. Deve ritirare, modificare o sospendere il trattamento quando la prognosi limitata lo giustifica. Deve adattare i test diagnostici e le misure terapeutiche e di supporto alla situazione clinica del paziente. Deve evitare l’inutilità, sia quantitativa che qualitativa.
3. Il medico, dopo aver informato adeguatamente il paziente, deve tenere conto della volontà del paziente di rifiutare qualsiasi procedura, compresi i trattamenti che prolungano la vita.
4. Quando le condizioni del paziente non gli consentono di prendere decisioni, il medico deve prendere in considerazione, in ordine di preferenza, le indicazioni precedentemente espresse dal paziente, le istruzioni precedenti del paziente e l’opinione del paziente attraverso i suoi rappresentanti. È dovere del medico collaborare con coloro che hanno il compito di garantire l’attuazione delle volontà del paziente”.
– Articolo 59 del Capitolo XIV sulla ricerca medica;
“1.La ricerca medica è necessaria per il progresso della medicina ed è un bene sociale che va promosso e incoraggiato. La ricerca che coinvolge soggetti umani dovrebbe essere condotta quando il progresso scientifico non è possibile con mezzi alternativi di pari efficacia o nelle fasi della ricerca in cui è indispensabile.
2.‐Il medico di ricerca deve prendere tutte le precauzioni possibili per preservare l’integrità fisica e psicologica dei soggetti di ricerca. È necessario prestare particolare attenzione alla protezione degli individui appartenenti a gruppi vulnerabili. Il bene dell’essere umano coinvolto nella ricerca biomedica deve prevalere sugli interessi della società e della scienza.
3.- Il rispetto per il soggetto della ricerca è il principio guida della ricerca. È sempre necessario ottenere il loro consenso esplicito. Le informazioni devono contenere almeno: la natura e lo scopo della ricerca, gli obiettivi, i metodi, i benefici attesi, nonché i potenziali rischi e disagi che la partecipazione può comportare. I clienti devono inoltre essere informati del loro diritto di non partecipare. o di ritirarsi liberamente in qualsiasi momento dall’indagine, senza subire alcun pregiudizio.
4.- Il ricercatore medico ha il dovere di pubblicare i risultati delle sue ricerche attraverso i normali canali di divulgazione scientifica, siano essi favorevoli o sfavorevoli. Non è etico manipolare o nascondere i dati, sia per un tornaconto personale o di gruppo, sia per motivi ideologici.
“La Dichiarazione WMA di Lisbona sui diritti del pazientee del 1981,“Ogni paziente ha il diritto di essere visitato da un medico che sa essere libero di dare un parere clinico ed etico, senza alcuna interferenza esterna.El paciente tiene derecho a la autodeterminación y a tomar libremente las decisiones que le afecten. Il medico deve informare il paziente delle conseguenze della sua decisione.
Il paziente adulto mentalmente competente ha il diritto di dare o negare il consenso a qualsiasi esame, diagnosi o terapia. Il paziente ha il diritto di ricevere le informazioni necessarie per prendere le proprie decisioni. Il paziente deve capire chiaramente qual è lo scopo di ogni esame o trattamento e quali sono le conseguenze del mancato consenso”.
La Dichiarazione della WMA sull’indipendenza e la libertà professionale del medico del 1986, secondo la quale: “I medici dovrebbero godere di una libertà professionale tale da consentire loro di curare i propri pazienti senza interferenze.
Il privilegio del medico di usare il giudizio professionale e la discrezione nel prendere le decisioni cliniche ed etiche necessarie per la cura e il trattamento dei suoi pazienti deve essere mantenuto e difeso. Garantendo l’indipendenza e la libertà professionale dei medici nell’esercizio della professione, la comunità assicura ai cittadini la migliore assistenza medica, che a sua volta contribuisce a creare una società forte e sicura.
La Dichiarazione di Madrid del 2009 della WMA sulla regolamentazione professionale riafferma la Dichiarazione di Seoul sull’autonomia professionale e l’indipendenza clinica dei medici, prevedendo che
“I medici godono di un elevato grado di autonomia professionale e di indipendenza clinica, per cui possono formulare raccomandazioni basate sulla loro conoscenza ed esperienza, sulle evidenze cliniche e sulla comprensione olistica dei pazienti, compreso ciò che è meglio per loro, senza influenze esterne indebite o inappropriate”.
I principi universali che permeano tutte le normative devono essere conformi al rispetto delle leggi umanitarie insite nell’inconscio collettivo, come recita la massima del giuramento di Ippocrate “…”.MANTENERE il massimo rispetto per la vita umana fin dal suo inizio, anche sotto minaccia, e non usare le conoscenze mediche contro le leggi dell’umanità.”
I valori etici hanno la precedenza sulle disposizioni legali limitanti, come riconosciuto nella Dichiarazione della WMA del 2003 sul rapporto tra legge ed etica, che prevede “Quando la legislazione e l’etica medica sono in conflitto, i medici devono cercare di far cambiare la legislazione. In caso di conflitto, le responsabilità etiche prevalgono sugli obblighi legali.
Quando un paziente affetto da una malattia cerca sollievo o di salvarsi la vita e chiede di provare un’opzione terapeutica per la quale ci sono indicazioni di utilità, come nel caso del Diossido di Cloro (ClO 2), è dovere del medico sostenere il paziente, acquisire conoscenze, condurre ricerche e diffonderle in conformità con l’articolo 27 della Dichiarazione universale dei diritti dell’uomo del 1948, in modo che tutti possano beneficiare del progresso scientifico, le informazioni devono essere liberamente condivise e diffuse in tutti i Paesi senza restrizioni, “…”.Ogni individuo ha il diritto di partecipare liberamente alla vita culturale della comunità, di godere delle arti e di condividere il progresso scientifico e i suoi benefici”.
Alla luce del momento storico affrontato da tutta l’umanità con la plandemia di Coronavirus e l’urgente necessità di salvare vite umane, dei recenti sviluppi relativi al trattamento del COVID-19 sia in ambito medico che accademico, e soprattutto dello scopo di questo documento, che è quello di fornire alle autorità le informazioni corrette sul diossido di cloro per un uso umano corretto e sicuro, vale la pena di riflettere su alcune questioni fondamentali relative ai diritti umani e alla pratica medica:
L’adesione a qualsiasi trattamento dipende dal tacito accordo e dalla collaborazione tra le parti: il medico e il paziente (o il tutore del paziente in condizioni particolari che non consentono una scelta consapevole dell’intervento medico, ad esempio situazioni di perdita di memoria, di incoscienza indotta da trauma o da trauma nei bambini). Il presente accordo è concordato liberamente e spontaneamente;
Sulla base della sua esperienza clinica, il medico è libero di prescrivere ciò che ritiene appropriato per il paziente, comunicando sempre il modo corretto di utilizzare un farmaco, i potenziali benefici e i rischi di un intervento terapeutico. D’altra parte, il paziente, sulla base delle spiegazioni fornite, delle convinzioni personali e delle informazioni complementari, è anche libero di accettare o meno qualsiasi forma di trattamento indicato;
La pratica medica dovrebbe sempre basarsi, quando possibile, su dati scientifici a sostegno degli approcci diagnostici e terapeutici utilizzati. Tuttavia, nelle situazioni in cui l’evidenza scientifica non è disponibile o è inaffidabile, spetta al medico utilizzare le proprie conoscenze, l’esperienza precedente e il buon senso per condurre la situazione clinica nel modo che gli sembra più appropriato. In questo caso, è importante che il medico chieda al paziente di firmare un documento di consenso libero e informato (TCLI). Per questa condotta, il Medico si basa sulla Dichiarazione di Helsinki (articolo 37) che recita: “Nel trattamento di un singolo paziente, quando è stabilito che nessun intervento o altri interventi conosciuti sono stati inefficaci, il medico, dopo aver chiesto il parere di esperti, con il consenso informato del paziente o di un rappresentante autorizzato, può utilizzare un intervento non provato se, a giudizio del medico, offre la speranza di salvare la vita, ripristinare la salute o alleviare la sofferenza”.
In tutti i casi, le nuove informazioni devono essere registrate e, se del caso, rese pubbliche;
Rispetto a questi aspetti, non possiamo sottovalutare il fatto che non ci sono sufficienti evidenze in letteratura scientifica che indichino l’uso delle SCD per la profilassi o il trattamento eziologico dei casi di COVID-19 di qualsiasi gravità, se guardiamo, ad esempio, alla relazione tecnica dei medici dell’AEMEMI sull’efficacia del 97% del trattamento dei pazienti con COVID-19 in 4 giorni a Guayaquil/Ecuador (AEMEMI 2020). Vale la pena ricordare che si tratta del primo gruppo di ricerca al mondo che intende condurre uno studio epidemiologico con i CDS; un altro studio è stato registrato con il numero NCT043742 presso la US National Library of Medicine/National Institutes of Health, in Dr. Eduardo Insignares et al. al. e intitolato “Determinazione dell’efficacia del diossido di cloro orale nel trattamento della COVID-19”, seguito dalla trilogia di Aparicio et.al. con migliaia di pazienti.
In poche parole:
Alla luce di quanto sopra, sulla base delle prove qui presentate con evidente esperienza da parte di scienziati e professionisti della salute, nonché già ben dimostrate in articoli scientifici già pubblicati, si consiglia l’uso della soluzione di diossido di cloro (CDS), secondo lo standard del Dr. h.c. Andreas Ludwig Kalcker (2017), debitamente diluita e quindi rispettando le dosi sicure da quanto già noto dagli studi di tossicità, che secondo i rapporti dei medici di diversi Paesi si è dimostrata sicura per il consumo umano e inoltre efficace contro la COVID-19 se consumata correttamente secondo protocolli standardizzati a livello internazionale.
Come esempio dell’uso consapevole e compassionevole del diossido di cloro (ClO2), possiamo citare lo Stato Plurinazionale della Bolivia, dopo un prolungato processo di dibattito e risoluzione nell’ambito dell’esercizio dei diritti umani e della Legge di Partecipazione e Controllo Sociale, la popolazione ha richiesto attraverso i suoi rappresentanti dipartimentali e dell’assemblea nazionale la legge che consente l’autorizzazione alla produzione, alla distribuzione con controllo di qualità e all’uso compassionevole del biossido di cloro.
Ad oggi (13 settembre 2020) sono in corso di elaborazione 4 leggi dipartimentali e 1 legge nazionale; nella sede governativa di La Paz la legge è stata promulgata il 9 settembre 2020.ClO2
Associazioni ed enti:
Studi e pubblicazioni:
Ringraziamenti speciali:
Brevetti e collegamenti diretti:
Dichiarazioni e manuali:
Avvertenze e aggiornamenti:
Banche dati e risorse:
Link di accesso e data di accesso indicata:
Nota terapeutica sul biossido di cloro per COVID-19:
La responsabilità e le competenze assunte da ciascuno degli attori del Paese li hanno portati ad agire nel modo più efficace di fronte alla pandemia. Il personale sanitario, nell’ambito dell’etica e della deontologia medica, si assume la responsabilità di rispondere alle esigenze e alle richieste della popolazione; in questo caso particolare, la popolazione ha richiesto l’uso del diossido di cloro come trattamento preventivo e curativo.
Di fronte a una pandemia fuori controllo, i rappresentanti della popolazione (consigli di quartiere, gruppi civici, organizzazioni di base, associazioni, la Central Obrera Boliviana, Federazione dei Minatori Boliviani, membri dell’Assemblea Dipartimentale e Nazionale), questi ultimi hanno avuto l’obiettivo di elaborare, discutere e promulgare la Legge sulla produzione, l’uso e la distribuzione del diossido di cloro.
Infine, chiediamo alle società scientifiche e bioetiche e alle istituzioni di formazione accademica di unirsi a questo progresso nell’esercizio dei diritti umani di fronte alla decisione della popolazione di scegliere in modo autonomo ed equo.
Esenzione di responsabilità:
Queste informazioni non intendono sostituire la consulenza, la diagnosi o il trattamento di un medico professionista e sono intese solo a scopo informativo. In caso di emergenza medica, contattare immediatamente il servizio di emergenza. Non siamo responsabili del contenuto dei siti esterni collegati. Pur impegnandoci a mantenere le informazioni accurate e aggiornate, non ne garantiamo la completezza o l’accuratezza. La menzione di test, prodotti o procedure specifiche non implica l’approvazione. Per qualsiasi domanda su una condizione medica, consultare sempre un medico qualificato. L’uso di queste informazioni è a proprio rischio e pericolo. Non siamo responsabili di eventuali danni derivanti dalla sua applicazione.

Copyright © 2012-2025 - Andreas Ludwig Kalcker. Tutti i diritti riservati.
